Эктопированная поджелудочная железа (эктопия) — Заболевания.Ру
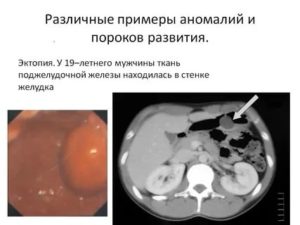
Аберрантная поджелудочная железа — это гетеротопия панкреатической железистой ткани в стенке желудка, кишечника или других органах брюшной полости. Аномалия характеризуется скудными клиническими проявлениями с преобладанием диспепсических расстройств.
Осложненные формы патологии манифестируют симптомокомплексом «острого живота», желудочно-кишечными геморрагиями. Диагностика основана на инструментальных методах: УЗИ, рентгенографии с пероральным контрастированием, ЭФГДС. Диагноз подтверждают патоморфологическим исследованием биоматериала.
Бессимптомные аномалии лечения не требуют, при осложнениях в основном прибегают к хирургическим вмешательствам.
Q45.3 Другие врожденные аномалии поджелудочной железы и протока поджелудочной железы
В медицинской литературе аномалия имеет ряд синонимов: добавочная поджелудочная железа, хористома, эктопия ПЖ.
Заболевание является самым частым пороком развития поджелудочной железы и выявляется у 0,2% пациентов в ходе оперативных вмешательств на органах брюшной полости. По данным аутопсий, гетеротопия встречается у 1,3% людей в популяции.
Аномалия в 2 раза чаще наблюдается у мужчин. Преимущественно она обнаруживается случайно в возрасте 40-70 лет при инструментальном обследовании пищеварительной системы.
Аберрантная поджелудочная железа
В современной гастроэнтерологии не существует единого мнения по поводу этиологических факторов. Большинство ученых утверждают, что патология возникает во внутриутробном периоде при сочетанном влиянии нескольких причин.
К наиболее вероятным из них относят спонтанные генетические мутации, инфекции, перенесенные матерью во время беременности.
Реже определяется связь аберрантной поджелудочной железы с приемом лекарств, обладающих тератогенным эффектом.
К факторам риска развития хористомы относят курение, употребление алкоголя и наркотических веществ беременной женщиной.
Вероятность появления болезни увеличивается при проживании в экологически неблагоприятных регионах, воздействии ионизирующего излучения на ребенка в эмбриональном периоде внутриутробного развития.
Риск формирования аберрантной ткани повышается при генетической предрасположенности — наличии различных аномалий у ближайших родственников.
Точный механизм образования аномалии до сих пор остается неясным. Наиболее вероятно, что аберрантная ткань — проявление атавизма в онтогенезе.
Нарушение закладки и дифференцировки поджелудочной железы при антенатальном развитии приводит к аномальному расположению части органа.
Сформированная добавочная железа имеет изолированное кровоснабжение и иннервацию, функционирует независимо от основной массы железистых клеток.
Хористомы различаются по анатомической локализации. Аберрантная ткань железы может располагаться в различных органах:
- двенадцатиперстной кишке (31,83%);
- стенке желудка (31,46%);
- тощей кишке (21,7%);
- подвздошной кишке (9,36%);
- брыжейке (3,37%);
- желчных ходах (1,49%).
Среди желудочных аберрантных ПЖ большинство (58,2%) располагается в привратнике. По макроскопическим признакам выделяют 4 формы: узловатую, полипозную, диффузную и смешанную.
Подавляющее большинство гетеротопий протекает бессимптомно и выявляется случайно при гастроэнтерологической диагностике, проведении операций в полости живота.
Симптоматика обычно возникает при осложненном течении заболевания и определяется локализацией аберрантной поджелудочной железы.
Начальными признаками являются неспецифические диспепсические расстройства: тяжесть в животе после приема пищи, тошнота, неустойчивость стула.
Клиническое проявление крупной аберрантной железы возможно уже в раннем детском возрасте.
Беспокоит срыгивание после еды, периодически бывает обильная рвота створоженным молоком или частично переваренной пищей. Дети плохо едят, медленно набирают вес, отстают в физическом развитии.
Во взрослом возрасте аномалия, как правило, протекает под маской хронического гастрита, панкреатита, холецистита.
Типичный симптом осложненных форм патологии — сильные боли в животе различной локализации. Часто встречается рвота с примесями слизи и желчи. При поражении желчевыводящих протоков выделяется обесцвеченный кал. Редко аберрантная поджелудочная железа манифестирует желудочно-кишечным кровотечением, которое проявляется кровавой рвотой или меленой.
Зачастую при хористоме наблюдается стеноз пилорического отдела желудка, что затрудняет продвижение пищи в тонкий кишечник. В компенсированной стадии питание и энергетический обмен практически не нарушены.
На этапе декомпенсации характерны истощение больных, анемия и признаки авитаминозов.
При расположении аберрантной ткани в тонком кишечнике существует вероятность развития острой кишечной непроходимости, требующей неотложной хирургической помощи.
Добавочные поджелудочные железы часто подвергаются воспалению и некрозу. Начинается асептическое либо гнойное поражение аберрантной ткани, которое чревато прободением стенки пораженного органа.
При расплавлении сосудистых стенок может открыться профузное кровотечение. Наличие гетеротопии повышает риск возникновения язвенной болезни, механической желтухи.
Наиболее опасное последствие вовремя не диагностированной хористомы — малигнизация.
Выявление аберрантной железистой ткани стандартными методами исследования затруднительно, поскольку внешне аномальные образования напоминают доброкачественную опухоль.
Для верификации диагноза врач-гастроэнтеролог назначает инвазивные методики с последующим гистологическим подтверждением.
При подозрении на гетеротопию поджелудочной железы диагностический поиск включает следующие исследования:
- УЗИ брюшной полости. При сонографии возможно обнаружение аберрантной ткани только большого объема, которая визуализируется в виде гиперэхогенных участков в нетипичных местах. Результаты УЗИ не позволяют установить природу объемного образования. Чтобы оценить кровоток в добавочной поджелудочной железе, рекомендована допплерография.
- Рентгенологические методы. При рентгенографии пассажа бария по ЖКТ гетеротопия выглядит как округлый дефект наполнения. При осложненной форме заболевания на фоне дефекта выявляют нишу или пятно бария. Аберрантную поджелудочную железу можно увидеть при компьютерной томографии ОБП.
- ЭФГДС. При эндоскопическом осмотре хорошо заметны хористомы, локализованные в желудке или начальных отделах 12-перстной кишки. Они имеют вид полипов или отдельных узлов, на поверхности которых зачастую есть устье выводного протока.
- Изучение биоптатов. Морфологический анализ образца тканей является решающим при диагностике хористом. По гистологическому строению добавочная железистая ткань может полностью соответствовать нормальной либо содержать отдельные элементы — островки Лангерганса, ацинусы или выводные протоки.
- Лабораторные методы. Анализы имеют вспомогательный характер. Для оценки внешнесекреторной функции поджелудочной железы определяют уровень амилазы, липазы и трипсина в крови. В образцах кала исследуют количество фекальной эластазы. В крови измеряют содержание глюкозы натощак, проводят глюкозотолерантный тест.
В гастроэнтерологии есть успешный опыт применения аналогов гормона соматостатина.
Эти препараты тормозят пролиферацию железистых клеток, препятствуют трансформации доброкачественной гетеротопии в опухолевый процесс.
При недостаточной экзокринной функции поджелудочной ткани назначают заместительную ферментную терапию. Для устранения неприятных симптомов используют анальгетики, желчегонные препараты, прокинетики.
Хирургическое лечение
В абдоминальной хирургии целесообразность оперативного вмешательства при аберрантной поджелудочной железе остается предметом научных дискуссий. При бессимптомном течении и нормальном функционировании органа с железистой геторотопией больным требуется наблюдение. Возможность проведения операции решается индивидуально для пациентов со сниженной функциональной активностью основной ПЖ.
Абсолютными показаниями к выполнению радикального лечения считают осложненные варианты аберрантной аномалии. Рекомендована максимально экономная резекция в пределах здоровых тканей. При формировании стеноза привратника или кишечника обеспечивается хирургическая коррекция, при необходимости накладывается анастомоз. Обязательному удалению подлежат хористомы с высоким риском малигнизации.
Бессимптомные формы аберрантной ПЖ не представляют риска для здоровья и жизни человека, в таком случае прогноз считается благоприятным. Прогностически неблагоприятно расценивается появление осложнений со стороны желудка, кишечника, билиарной системы, быстрое увеличение размеров добавочной железы. Учитывая неясный этиопатогенез, специфические меры первичной профилактики не разработаны.
Источник: //www.KrasotaiMedicina.ru/diseases/zabolevanija_gastroenterologia/aberrant-pancreas
Способ лечения аберрантной поджелудочной железы, расположенной в желудке
Изобретение относится к медицине, а именно к эндоскопическому лечению аберрантной поджелудочной железы, расположенной в желудке, в том числе и у детей.
Известен способ хирургического лечения аберрантной поджелудочной железы (Маев И.В., Кучерявый Ю.А. Клинические перспективы в гастроэнтерологии, гепатологии. 2005. №3. С.24-30), включающий оперативное лечение с иссечением аберрантной поджелудочной железы путем полнослойной резекции участка желудка.
Недостатком этого способа является то, что способ является травматичным и требует проведения лапаротомии с последующим нахождением в стационаре до 10 суток.
В настоящее время наиболее распространенным способом лечения аберрантной поджелудочной железы является – минилапаротомия с эндоскопической поддержкой.
При выполнении оперативного вмешательства, учитывая локализацию аберрантной поджелудочной железы, проводится иссечение образования со стенкой желудка. (Винокурова Н.В. Автореф. На соиск. уч. степ. к.м.н.
Диагностика и хирургическое лечение эктопии поджелудочной железы в стенку желудка у детей. 2009. С.24, прототип).
Недостатком данного способа является то, что минилапаротомия и лапароскопия являются внутриполостным оперативным вмешательством, требующим разреза передней брюшной стенки под эндотрахеальным наркозом, нахождения в стационаре не менее 7 суток с последующей реабилитацией в послеоперационном периоде.
Задачей настоящего изобретения является устранение указанных недостатков, снижение травматичности операции, за счет сохранения целостности передней брюшной стенки и серозной стенки желудка.
Для достижения поставленной задачи, в способ лечения аберрантной поджелудочной железы, расположенной в желудке, включающем ее удаление под видеоконтролем, предложено осуществлять гастроскопию.
При этом проводят через гастроскоп коагуляционный зонд, посредством которого осуществляют коагуляцию области протока аберрантной поджелудочной железы с формированием канала на всю ее толщину.
Затем послойно коагулируют ткани аберрантной поджелудочной железы в направлении от ее периферии к области сформированного канала, после чего воздействуют на операционную область NO-терапией в терапевтическом режиме в течение 1-2 минут.
То, что не рассекается серозная оболочка желудка, исключает возможность развития воспаления брюшины. Применение коагуляции уменьшает кровопотерю при удалении аберрантной поджелудочной железы, а NO-терапия способствует заживлению с формированием недеформирующего рубца.
На фиг.1 представлена УЗИ сканограмма аберрантной поджелудочной железы в стенку желудка.
Способ осуществляется следующим образом.
Проводится определение границы железы при помощи УЗИ и диагностической гастроскопии. Далее с помощью гастроскопа в апикальной части железы коагуляционным зондом формируется канал в области протока аберрантной поджелудочной железы, который четко визуализируется, на всю ее глубину.
Затем с помощью эндоскопической инъекционной иглы или коагуляционного зонда от периферии к центру с помощью электрокоагулятора проводится деструкция с удалением аберрантной поджелудочной железы. Для достижения полного удаления аберрантной поджелудочной железы требуется 1-2 манипуляции.
После этого через канал гастроскопа осуществляют воздействие на патологический очаг воздушно-газовым потоком, содержащим 1000-3000 мг/м3 монооксида азота с температурой 20-30°C в терапевтическом режиме в течение 1-2 минут.
Все манипуляции проводятся под контролем фиброэндоскопа, что сводит к минимуму возможности развития осложнений предложенной методики лечения.
В дальнейшем 1 раз в 6 месяцев, в течение 2-х лет, проводится динамическое УЗИ и эндоскопическое наблюдение.
Осуществление способа показано на конкретном клиническом примере.
Пример 1.
Больной Б., 13 лет (ист. Бол. №15365, 2006 г.), поступил в отделение детской хирургии с диагнозом: аберрантная поджелудочная железа в стенку желудка.
При помощи УЗИ и гастроскопии определили границу аберрантной железы (фиг.1). По вышеописанной методике провели поэтапное удаление аберрантной поджелудочной железы посредством пуговчатого коагуляционного зонда.
Затем через канал эндоскопа осуществили воздействие на патологический очаг воздушно-газовым потоком, содержащим 1000-3000 мг/м монооксида азота с температурой 20-30°C в терапевтическом режиме в течение 2 минут.
Все манипуляции проводили под контролем фиброэндоскопа.
Для достижения полного удаления аберрантной поджелудочной железы потребовалось 2 манипуляции. Динамическое наблюдение в течение 5 лет показало полное выздоровление.
По предлагаемому способу провели лечение 15 больных. Обследование в отдаленные сроки показало, что у всех пациентов аберрантная поджелудочная железа полностью удалена.
Способ позволяет выполнить мини инвазивное удаление аберрантной поджелудочной железы, повысить эффективность лечения, провести социальную реабилитацию больных, исключить риск малигнизации и восстановить работоспособность.
Способ лечения аберрантной поджелудочной железы, расположенной в желудке, включающий ее удаление под видеоконтролем, отличающийся тем, что осуществляют гастроскопию, проводят через гастроскоп коагуляционный зонд, посредством которого коагулируют область протока аберрантной поджелудочной железы с формированием канала на всю ее толщину, затем послойно коагулируют ткани аберрантной поджелудочной железы в направлении от ее периферии к области сформированного канала, после чего воздействуют на операционную область NO-терапией в терапевтическом режиме в течение 1-2 мин.
Источник: //findpatent.ru/patent/249/2495631.html
Источник: https://zabolevan.ru/ektopirovannaya-podzheludochnaya-zheleza-ektopiya.html
Острая тонкокишечная непроходимость, вызванная эктопированным участком поджелудочной железы. Клинический случай
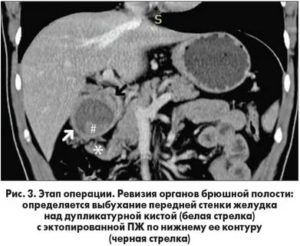
Эктопия поджелудочной железы — это аномалия, связанная с необычным расположением панкреатической ткани с собственным кровоснабжением и протоками. Она не имеет анатомического, сосудистого и нервного контакта с нормально расположенной поджелудочной железой [1].
Добавочная (аберрантная) поджелудочная железа (ПЖ) — самый частый порок развития железы, который заключен в гетеротопии ее ткани в стенку желудка, кишечника, желчного пузыря, дивертикул Мек- келя, печень, селезенку и, значительно реже, в другие органы без связи с основной поджелудочной железой [2, 3].
Аберрантная ПЖ по своим проявлениям неспецифична, в значительной степени клиническая картина зависит от локализации и размера гетеротопии и чаще всего появляется при развитии осложнений, к которым относят воспаление, некроз, перфорацию желудочной или кишечной стенки, кровотечение, кишечную непроходимость — которую мы хотим представить в виде клинического примера.
Рисунок 1. Обзорная рентгенография органов брюшной полости — картина острой тонкокишечной непроходимости
Figure 1. Plain abdominal X-ray presenting acute small intestinal obstruction
Рисунок 2. Ультразвуковая картина инвагинации кишечника
Figure 2. Intestinal intussusception, ultrasound imaging
Клинический случай
Описан случай острой тонкокишечной непроходимости, вызванной эктопированной тканью поджелудочной железы в стенку тонкой кишки.
Больной Б., 39 лет, доставлен скорой помощью в приемное отделение хирургии ГКБ № 13 г. Уфы с жалобами на приступообразные боли в животе, тошноту, однократную рвоту, вздутие живота, слабость.
Заболел около 4-х часов назад, когда появился сначала дискомфорт в животе, в области эпигастрия. В динамике боли в животе усилились, начали носить приступообразный характер. Принимал лекарственные препараты из группы нестероидных противовоспалительных средств.
До госпитализации обращался в частную клинику, где периодически обследовался и находился на амбулаторном лечении в течение 4-х месяцев, и был направлен на скорой помощи в ГКБ № 13 с направительным диагнозом «Перфоративная язва двенадцатиперстной кишки», так как в анамнезе у больного отмечалась язвенная болезнь двенадцатиперстной кишки.
При осмотре — состояние средней тяжести. Кожные покровы, видимые слизистые чистые, бледноватой окраски. Язык суховат, обложен серым налетом. Живот умеренно вздут, при пальпации мягкий, болезненный преимущественно в нижних отделах живота. Симптомов раздражения брюшины нет. Перистальтика кишечника усилена.
Печень у края реберной дуги. Печеночная тупость сохранена. Стул самостоятельный жидкий, накануне, естественной окраски. Газы не отходили. Мочеиспускание не нарушено. Per rectum: сфинктер в тонусе. Ампула прямой кишки пустая. Патологических образований на высоте пальца не определяется.
На перчатке следы кала естественной окраски.
Больной обследован в приемном отделении: ОАК: эр. 4,2х1012/л, Hb 128 г/л, Ht 37,3 %, тр. 221,0х109/л, Л 8,3х109/л; биохимический анализ крови: общий белок 57,0 г/л, мочевина 2,8 ммоль/л, креатинин 69,3 ммоль/л, билирубин общий 8,0 мкмоль/л, глюкоза 10,5 ммоль/л, АЛТ 8,6 Е/л, АСТ 16,8 Е/л.
Обзорная рентгенография органов брюшной полости показала чаши Клойбера, арки, преимущественное расположение — левые отделы брюшной полости (рис. 1). На УЗИ ОБП — картина инвагинации кишечника на фоне выраженного пневматоза и гиперперистальтики, на левой половине правого рисунка — поперечная проекция инвагинации, так называемый «бутон розы» (рис. 2).
Принято решение о диагностической лапароскопии.
На лапароскопии — в брюшной полости серозный выпот до 40 мл, вздутые петли тонкой кишки, при ревизии обнаружен тонко-тонкокишечный инвагинат (рис. 3). Учитывая опасность повреждения стенки тонкой кишки, выполнена конверсия.
Рисунок 3. Диагностическая лапароскопия. Тонкокишечный инвагинат
Figure 3. Diagnostic laparoscopy, small intestine intussusceptum
Рисунок 4. Фрагмент тонкой кишки и полиповидное образование, представленное гетеротопиро- ванными участками поджелудочной железы, состоящими из ацинусов и протоков, располагающихся между мышечными тяжами, с обширными кровоизлияниями и некрозами. Слева ацинусы и протоки поджелудочной железы, справа — эпителий тонкой кишки. Окраска по Ван-Гизону
Figure 4. Small intestinal fragment with the polyp- neoplasm: heterotypic pancreatic foci (with acini and ducts) located between muscular bands, with extensive areas of haemorrhaging and necrosis. On the left — pancreatic acini and ducts, on the right — small intestine epithelium
Произведена средне-срединная лапаротомия, в тонкой кишке на расстоянии 240 см от связки Трейтца определяется инвагинат. С техническими трудностями произведена дезинвагинация.
При ревизии тонкой кишки, вовлеченной в инвагинацию, перистальтика и пульсация прослеживаются, кишка признана жизнеспособной.
В просвете данного участка тонкой кишки пальпируется округлой формы образование размерами 6,0х1,5х1,5 см, которое внешне напоминает дивертикул Меккеля, инвагинированный в просвет кишки.
Произведена клиновидная резекция тонкой кишки с данным образованием, с ушиванием просвета кишки двухрядным узловым швом. Данное образование и вызвало непроходимость тонкой кишки, явившееся этаким «грузилом», запустившим механизм инвагинации.
Результаты
Послеоперационный период гладкий, больной выписан на девятые сутки после хирургического вмешательства после снятия кожных швов.
Нас удивил результат патоморфологического исследования материала. В материале — фрагмент тонкой кишки и полиповидное образование, представленное гете- ротопированными участками поджелудочной железы, состоящими из ацинусов и протоков, располагающихся между мышечными тяжами, с обширными кровоизлияниями и некрозами.
Таким образом, можно говорить о развитии панкреатита добавочной поджелудочной железы в течение нескольких месяцев, обструкция выводных протоков которой вызвала отек и воспаление, что, в свою очередь, запустило механизм инвагинации тонкой кишки.
При контрольном осмотре через два месяца — жалоб не предъявляет, самочувствие у больного хорошее, дискомфорт, периодические боли в животе, беспокоившие его несколько месяцев до поступления в стационар, купировались. Послеоперационный рубец в удовлетворительном состоянии. На УЗИ органов брюшной полости без значимой патологии. Уровень глюкозы крови в пределах нормы.
Ближайшие результаты проведенного лечения оцениваются как хорошие.
Обсуждение
Впервые описание дополнительной поджелудочной железы предоставил Шульц (1727), который обнаружил ее в дивертикуле Меккеля.
Существуют описания ассоциации аберрантной ПЖ, локализующейся в дивертикуле Меккеля, в сочетании с болезнью Крона, при этом эктопированная железа не проявлялась какими-либо самостоятельными симптомами.
Вероятно, данную связь следует признать случайной, по крайней мере в настоящее время.
При воспалении аберрантной ПЖ, локализующейся в дивертикуле Меккеля [4, 5], клиническая картина может имитировать острый аппендицит [6].
Первое гистологическое описание гетеротопии поджелудочной железы принадлежит J. Klob в 1859 г. К 1927 г. было описано 60 случаев добавочной поджелудочной железы. В последующие 20 лет — еще 415. В отечественной и зарубежной литературе к 1960 г. было описано 724 случая хористом.
Учитывая морфологическую картину, различают четыре варианта эктопии ПЖ:
- наличие всех ее компонентов;
- наличие только экзокринной части;
- наличие только островков;
- наличие одних протоков (аденомиоз).
В настоящее время частота встречаемости гетеротопии поджелудочной железы значительно увеличилась и составляет в среднем до 0,2 % при оперативных вмешательствах на органах брюшной полости и 0,5-13 % случаев при аутопсиях.
Такой существенный разброс статистических данных объясняют особенностями исследования секционного материала в разных прозектурах. Аберрантную ПЖ примерно вдвое чаще встречают у мужчин, чем у женщин.
Наиболее часто аберрантная ПЖ локализована в гастродуоденальной зоне (63-70 % от всех случаев гете- ротопии ПЖ) с преимущественным расположением в антральном и пилорическом отделах желудка (85-95 % всех случаев гетеротопии ПЖ в желудке) [7, 8].
В желудке аберрантная ПЖ чаще находится в подслизистом слое, ограничиваемая мышечной оболочкой, реже располагается субсерозно). В двенадцатиперстной и тощей кишке аберрантную железу встречают сравнительно реже: 9-36 % и 0,5-27 % случаев соответственно [9, 10].
Остальные локализации эктопии ПЖ: в стенку желчного пузыря, печень и внепеченочные желчные протоки, селезенку, дивертикул Меккеля обнаруживают не часто [11]. Достаточно редкой локализацией аберрантной ПЖ считают субсерозное расположение в тонкой кишке [12, 13], в стенке кисты ДПК, пищеводе. В исключительных случаях встречают гетеротопию ПЖ в легочную ткань, пупок и корень языка [14, 15].
Следует отметить, что при локализации в тонкой кишке бессимптомно протекает менее половины случаев, поскольку осложнения возникают несколько чаще [1].
Заключение
Диагностика эктопированной ткани поджелудочной железы в тонкую кишку является крайне сложной проблемой в абдоминальной хирургии и выявляется в большинстве случаев при развитии осложнений.
Для окончательной диагностики данного заболевания имеет огромное значение патоморфологическая верификация, которая позволяет правильно определить причину и механизм развития острого хирургического заболевания.
В нашем случае можно предположить, что своевременное хирургическое вмешательство у данного больного предупредило развитие возможных последующих осложнений эктопированной ткани поджелудочной железы в стенку тонкой кишки, таких как малигнизация, кишечное кровотечение, перфорация стенки кишки и перитонит.
1. Marques J., Castro J., Oliveira H. Ectopic pancreas: a less common presentation. Rev Portug Cir. 2015;(34):43.
2. Jang K.M., Kim S.H., Park H.J., Lim S., Kang T.W., Lee S.J., et al. Ectopic pancreas in upper gastrointestinal tract: MRI findings with emphasis on differentiation from submucosal tumor. Acta Radiol. 2013;54(10):1107–16. DOI: 10.1177/0284185113491251
Источник: https://www.surgonco.ru/jour/article/view/366?locale=ru_RU
Эктопия поджелудочной железы в стенку желудка

Желудок » Вопросы » Эктопия поджелудочной железы в стенку желудка
Санников О.Р. 1 , врач эндоскопист, к.м.н.
Морозов С.Л. 2 , врач патологоанатом
1 ФБУЗ МСЧ №41 ФМБА России, г. Глазов
Гетеротопия (heteros – другой, topos – место) – порок развития ткани, появляющейся в необычном для нее месте.
Гетеротопия, аберрация или эктопия поджелудочной железы (ПЖ) определяется как топографическая аномалия панкреатической ткани вне связи с нормальной ПЖ [4]. Является относительно редкой врожденной аномалией – 0.55-13.7% по результатам аутопсий, средняя частота встречаемости в популяции 1-2% [4,5].
На каждые 500 хирургических вмешательств на органах верхних отделов желудочно-кишечного тракта приходится одна эктопированная ПЖ как случайная находка [4].
Гетеротопия ПЖ встречается у больных любого возраста, у мужчин в 2 раза чаще, чем у женщин, и не имеет клинических проявлений, однако, в некоторых случаях эктопированная ткань может проявлять симптоматику, характерную для заболеваний ПЖ, таких как панкреатит, цисты и псевдоцисты, нейроэндокринные и злокачественные опухоли [6,7,8-10].
Такую аномалию описывают как аберрантную гетеротопическую, дистопированную поджелудочную железу, панкреатическую лимфаденому, хористому, хористобластому.
Чаще дополнительная ПЖ обнаруживается в органах, имеющих общий с ней зачаток, или в тканях, взаимодействующих в процессе роста с зачатками поджелудочной железы, что позволяет рассматривать эктопированную поджелудочную железу как проявление дизонтогенетической гетеротопии.
В 90% наблюдений эктопированная ткань ПЖ локализуется в верхних отделах ЖКТ – в желудке, двенадцатиперстной, поперечной ободочной кишках, желчевыводящих путях, селезенке, брыжейке. Наиболее часто она встречается в гастродуоденальной зоне – 63 – 70% всех локализаций, излюбленный сегмент – антральный отдел желудка [3]. Реже встречается в подвздошной кишке, дивертикуле Меккеля, пищеводе, печени, желчном пузыре, сальнике, легких, средостении, маточных трубах и пупке [6,7]. В большинстве случаев гетеротопия ПЖ носит одиночный характер.
Макроскопически при эндоскопическом исследовании аберрантная ПЖ представляет собой опухолевидное образование округлой или овальной формы, размером от нескольких миллиметров до 4–5 см, на широком основании, располагающееся в подслизистом слое желудочной стенке.
На его вершине имеется выводной проток в виде пупковидного вдавления, открывающийся на слизистой оболочке желудка (фото 1). Встречаются формы, внешне больше напоминающие вид мелкого дивертикула (фото 2). При инструментальной пальпации аберрантная поджелудочная железа имеет плотную консистенцию [3].
Диаметр ее колеблется от нескольких миллиметров до 6 – 7 см, масса – от 4 до 16 г.
Элементы ткани поджелудочной железы чаще всего выявляются в подслизистом, реже – в мышечном и субсерозном слоях стенки желудка [2].
При гистологическом исследовании материала гетеротопия тканей ПЖ может быть представлена всеми ее компонентами в виде типичной ацинарной ткани обычного долькового строения, протоков (часто множественных, извитых, неравномерно расширенных, анастомозирующих) и панкреатических островков.
При этом протоки большей своей частью располагаются вне ацинарной ткани, иногда обнаруживаются множественные скопления, выстланы высоким призматическим однослойным эпителием без признаков атипии. Элементы островкового аппарата часто можно обнаружить вне основного узла. Различают четыре варианта эктопии ПЖ:
- определяются все компоненты поджелудочной железы;
- имеется только экзокринная часть органа;
- определяется только островковый аппарат;
- имеются одни протоки (аденомиоз).
Почти в 40% наблюдений находят одновременно ацинусы, протоки и железы, напоминающие дуоденальные [1].
Приводим собственное клиническое наблюдение случая.
Пациентка В., 59 лет обратилась к нам в связи обнаруженным “полипом” ДПК во время предыдущего исследования. Жалоб не предъявляет.
ЭГДС: Пищевод, желудок – без особенностей
ДПК: Слизистая верхнего дуоденального изгиба и нисходящей ветви ДПК с множественными милиарного типа высыпаниями, напоминающие «манную крупу», располагающимися преимущественно на поверхности керкринговых складок, фатеров сосок не визуализируется, продольная складка не напряжена. Пристеночно небольшое количество неизмененной желчи.
St.loc.: в зоне apex bulbi duodeni, близ сфинктера Капанджи, располагаясь на передней стенке, визуализируется крупный дефект полиповидного (0-Ip) типа на хорошо выраженной ножке размеры (фото 3,4) его ориентировочно составляют 1.2х1.3х2.0-2.3-2.
5 см: цвет практически не отличается от окружающей низмененной слизистой, поверхность в области головки образования с экссудативными изменениями, порыта слизью, поверхностный рисунок, характерный для аденом, отсутствует, слизистая напоминает окружающую; дефект очень подвижен, легко смещается в pars descendens и обратно в луковицу во время антиперистальтических волн, эластичность ткани не изменена, видимых перифокальных инфильтративных изменений не прослеживается, четко определить характер роста (субмукозный, эпителиальный) визуально не представляется возможным. В основание ножки дефекта введено
20 мл смеси р-ра адреналина 0.
1% и физраствора в соотношении 1:20, создана зона анемизации, отмечается побледнение ножки и прилежащей к ней слизистой apex bulbi duodeni, чередованием режимов резания-коагуляции полип отсечен, извлечен д\патоморфологического исследования.
На ревизии: культя с синюшным оттенком высотой до 1.0 см, зона резекции вполнена фибринозным экссудатом, на ее поверхности — темный, слегка втянутый участок неправильной формы (гематин), кровотечение отсутствует (фото 5).
| Рис 1 | Рис 2 | Рис 3 |
| Рис 4 | Рис 5 |
Заключение: Эндоскопическое внутрипросветное оперативное вмешательство: солитарное субэпителиальное (эпителиальное?) образование полиповидного (0-Ip) типа flex.duodenalis superior (фиброаденома? лейомиома? карциноид? аденома?).
Эндоскопическая петлевая электроэксцизия образования с превентивной анемизацией зоны резекции.
Косвенные эндоскопические признаки “неблагополучия” органов панкреато-билиарной зоны (лимфагиоэктазии слизистой оболочки pars descendens duodeni).
В подслизистом слое стенки желудка определяются железистые структуры ацинарного характера, выстланные высоким призматическим однослойным эпителием (фото 6 объектив план х10, окраска гематоксилин-эозин).
Железистые образования формируют дольки, разделенные друг от друга тонкими соединительнотканными перегородками с очаговыми лимфоцитарными инфильтратами и расширенными протоками (фото 7 объектив план х10, окраска гематоксилин-эозин)
Таким образом, резюмируя, можно отметить, что в некоторых случаях эктопированная долька ПЖ макроскопически может проявлять себя не только в виде “классических форм” (протрузии, плоские возвышения с устьем выводного протока на верхушке), но и педункулярных образований, более характерных для аденом; во всех случаях такие образования должны подвергаться эндоскопической эксцизии и тщательной морфологической верификации.
Различные типы неопухолевых поражений могут проявляться в виде субэпителиальных новообразований, тем самым имитируя опухолевый процесс. К ним относят эктопическую поджелудочную железу, кистозный гастрит и амилоидому.
Эктопическая поджелудочная железа (гете-ротопическая, добавочная, или аберрантная, поджелудочная железа) — ткань поджелудочной железы, которая не связана анатомически с самой железой и имеет отдельное от нее кровоснабжение.
Эктопические участки обычно располагаются в желудке, двенадцатиперстной и тощей кишке (Kim et al., 2009).
При дифференциальной диагностике с субэпителиальными опухолями, такими как ГИСО и лейомиома, учитывают сочетание следующих КТ-признаков (Kim et al., 2009): — активное контрастирование вышележащей слизистой оболочки — антральное или дуоденальное расположение — высокий индекс соотношения длинной оси к короткой оси — эндофитный тип роста
— нечеткие границы поражения.
При кистозном гастрите выявляют эктопическую пролиферацию железистых структур желудка, чаще они располагаются глубже, чем в норме. Кистозный гастрит желудка — редкая патология подслизистого слоя, которая чаще всего возникает при наличии желудочно-кишечного анастомоза. Однако иногда она возникает и при отсутствии предшествующих операций на желудке.
Гистологически поражение распространяется в подслизистый слой желудка и состоит из удлиненных гипреплазированных желудочных ямок с гиперплазией и кистозной дилатацией желез желудка.
При таком поражении выявляют гигантские складки желудка, подслизистое образование или изолированный полип (кистозный полипозный гастрит).
КТ-проявления кистозного гастрита могут варьировать от гомогенно накапливающего контраст полипа до только кистозного субэпителиального поражения.
1. К субэпителиальным поражениям желудка относят различные типы опухолевых и неопухолевых заболеваний.
2. Самая распространенная субэпителиальная опухоль желудка— гастроинтестинальная стромальная опухоль (ГИСО).
3. Наиболее частое место возникновения ГИСО — желудок, следующие по частоте — тонкая кишка, колоректальная зона, пищевод, сальник и брыжейка.
4. Риск агрессивного клинического течения ГИСО желудка определяют на основании размера опухоли и митотического индекса.
5. Злокачественность процесса позволяют заподозрить такие КТ- или MPT-признаки, как размер (> 5 см), гетерогенное накопление контраста и некроз.
6. Наличие увеличенных лимфатических узлов в перигастральной или отдаленных регионах — дифференциальный признак, позволяющий отличить шванному от ГИСО.
7. Лейомиома желудка в основном локализуется в области кардии, и при КТ ее визуализируют в виде гомогенного гиподенсивного субэпителиального образования.
8. Отличительные КТ-признаки гломусных опухолей, позволяющие дифференцировать их от других субэпителиальных образований желудка, — расположение главным образом в антральном отделе, накопление контраста подобно гемангиоме при динамическом контрастировании, активное и постоянное накопление контраста в венозную фазу, утолщение вышележащей слизистой оболочки.
9. При дифференциальной диагностике эктопической поджелудочной железы с субэпителиальными опухолями, такими как ГИСО и лейомиома, учитывают сочетание следующих КТ-признаков: активное контрастирование вышележащей слизистой оболочки, антральное или дуоденальное расположение, высокий индекс соотношения длинной оси к короткой, эндофитный тип роста и нечеткие границы поражения.
Редактор: Искандер Милевски. 20.5.2019
Аннотация научной статьи по клинической медицине, автор научной работы — Румянцева Галина Николаевна, Минько Татьяна Николаевна, Трухачев Сергей Валентинович, Бревдо Юрий Феликсович, Светлов Владислав Викторович
В статье приводятся данные о механизме возникновения эктопированной поджелудочной железы, наиболее частых местах ее локализации.
На собственном материале авторы описали эктопию поджелудочной железы в стенку желудка (ЭПЖСЖ) у 29 детей , клинические проявления заболевания и методы диагностики, из которых основным является эзофагогастродуоденоскопия.
Диагноз ЭПЖСЖ окончательно верифицирует обнаружение ткани поджелудочной железы в операционном препарате при гистологическом исследовании.
Diagnostics and treatment of ectopic pancreas in children
Mechanism of formation of ectopic pancreas and its localization are discussed the observation of 29 children suffering pancreas ectopy into the gastric wall .
The clinical manifestations of the disease and methods of its diagnostics with special reference to esophagogastroduodenoscopy are described.
The diagnosis is definitively confirmed by finding pancreatic tissue in the intraoperatively obtained tissue samples available for histological studies.
1. Дронов А. Ф., Смирнов А. Н., Залихин Д. В. и др. // Хирургия. — 2009. — № 6. — С. 50—53.
2. Лёнюшкин А. И. // Дет. хир. — 1997. — № 1. — С. 31—37.
3. Лёнюшкин А. И. — М., 1999.
4. Поддубный И. В., Исаев А. А., Алиева Э. И. и др. // Дет. хир. — 2006. — № 3. — С. 7—8.
5. Поддубный И. В., Козлов М. Ю., Исаев А. А. и др. // Материалы VIII Российского конгресса «Современные технологии в педиа-
трии и детской хирургии». — М., 2009. — С. 313.
6. Разумовский А. Ю., Гераськин А. В., Дронов А. Ф. // Рос. вестн. дет. хир., анестезиол. и реаниматол. — 2010. — № 1. — С. 29—40.
7. Georgeson K. E., Cohen R. D., Herba A. et al. // Ann. Surg. —
1999. — Vol. 229, N 5. — P. 678—682.
8. Georgeson K. E., Inge T. H., Albanese C. T. // J. Pediatr. Surg. —
2000. — Vol. 35, N 6. — P. 927—930.
9. Gurran T. J., Raffensperger J. G. // J. Pediatr. Surg. — 1994. — Vol. 29. — P. 1273—1275.
10. Varni J. // Med. Care. — 2001. — Vol. 39. — P. 800—8l2.
ДИАГНОСТИКА И ЛЕЧЕНИЕ ЭКТОПИРОВАННОЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ У ДЕТЕЙ
Кафедра детской хирургии (зав. — проф. Г. Н. Румянцева) Тверской государственной медицинской академии; Детская областная клиническая больница (главный врач И. А. Бармин), Тверь
Румянцева Галина Николаевна, e-mail: peduroltv@list.ru, Минько Татьяна Николаевна, Трухачев Сергей Валентинович, Бревдо Юрий Феликсович, Светлов Владислав Викторович, Галахова Диана Ганиевна
В статье приводятся данные о механизме возникновения эктопированной поджелудочной железы, наиболее частых местах ее локализации.
На собственном материале авторы описали эктопию поджелудочной железы в стенку желудка (ЭПЖСЖ) у 29 детей, клинические проявления заболевания и методы диагностики, из которых основным является эзофагогастроду-оденоскопия.
Диагноз ЭПЖСЖ окончательно верифицирует обнаружение ткани поджелудочной железы в операционном препарате при гистологическом исследовании.
Ключевые слова: дети, эктопия поджелудочной железы в стенку желудка, оперативное лечение
Mechanism of formation of ectopic pancreas and its localization are discussed the observation of 29 children suffering pancreas ectopy into the gastric wall.
The clinical manifestations of the disease and methods of its diagnostics with special reference to esophagogastroduodenoscopy are described.
The diagnosis is definitively confirmed by finding pancreatic tissue in the intraoperatively obtained tissue samples available for histological studies.
Key words: pancreas ectopy into the gastric wall, surgical treatment, children
Источник: https://moy-zheludok.ru/voprosy/ektopiya-podzheludochnoj-zhelezy-v-stenku-zheludka






