Как лечить нарушение мозгового кровообращения

После 40-50 лет постепенно накапливается груз проблем и заболеваний.
Часть из них можно легко устранить за счет ведения здорового образа жизни, изменений питания и нагрузок, но когда нарушено кровообращение головного мозга, лечение должно быть специфическим, зависящим от вида патологии (острые или хронические расстройства), а также от степени тяжести и наличия определенных симптомов и осложнений.
В соответствии с данными ВОЗ патологии, связанные с сосудами, особенно острые, являются ведущей причиной инвалидизации и гибели относительно молодых пациентов.
Прогрессирующие симптомы хронического нарушения без медицинского вмешательства постепенно, на протяжении нескольких лет, приводят к прогрессирующей деменции в результате формирования ДЭП (дисциркуляторной энцефалопатии), с расстройствами как мыслительной деятельности, когнитивных функций, так и двигательных актов, чувствительности и координации. В связи с этим важным становится вопрос о том, как лечить данное заболевание при наличии острых расстройств или хронических, постепенно прогрессирующих отклонений. Этими вопросами занимаются нейрохирурги, неврологи и терапевты, которые сталкиваются с такими пациентами.
Нарушение мозгового кровообращения: симптомы, лечение острых и хронических форм
Если формируются симптомы этой патологии, терапия проводится исключительно в стационарных условиях, под присмотром врачей и медперсонала. Это важно для того, чтобы не упустить драгоценное время и минимизировать степень повреждения нервной ткани гематомой или ишемией.
Если вызов скорой помощи и доставка пациента с подозрениями на инсульт осуществляется в пределах первых 4-6 часов, прогнозы в отношении дальнейшего лечения и реабилитации будут наиболее благоприятными.
В этом периоде возможны мероприятия по лизису (принудительному растворению) тромба или по остановке кровотечения в области разрыва сосуда, что уменьшит тяжесть поражения и его размеры.
Начнем с того, что рассмотрим основные принципы, как лечить нарушение мозгового кровообращения. К ним относят вызов скорой помощи при подозрении на инсульт и госпитализация в неврологическое отделение или ОРИТ (отделение реанимации и интенсивной терапии).
- На начальном этапе проводятся действия по поддержанию жизнедеятельности всех внутренних органов, особенно сердечно-сосудистой системы и легочной вентиляции, важен контроль за давлением, чтобы повреждения при инсульте или ТИА (транзиторной ишемической атаке) не усиливались.
- Важны процедуры по борьбе с отеком и набуханием мозга, по обеспечению полноценного функционирования его оболочек. Проводится коррекция расстройств водно-солевого обмена за счет введения растворов, поддержание тонуса сосудов и снятие их спазма, коррекция реологических и свертывающих свойств крови.
- В дальнейшем терапия направлено на устранение причины, которая вызвала все произошедшие изменения, и на профилактику рецидива, проводятся реабилитационные мероприятия при наличии двигательных, чувствительных или когнитивных расстройств.
При наличии симптомов хронического расстройства, лечение осуществляется комплексно, с воздействием на основную причину проблемы и на нормализацию кровотока в артериях и венах всех органов. Целенаправленно применяются лекарственные препараты: внутрь, внутримышечно, внутривенно.
В комплекс процедур должны обязательно входить средства, нормализующие артериальное давление:
- базовая терапия;
- средства для профилактики кризов.
Важно также снижение холестерина и атерогенных липидных фракций — «вредных» жиров, способствующих формированию холестериновых бляшек на внутренней поверхности сосудов. Среди физиотерапевтических методик рекомендована магнитотерапия.
Проведение таких мероприятий улучшает показатели артериального давления, состояние сосудов, нормализует кровоток и способствует стабилизации показателей. В связи с этим постепенно улучшается сон и общее самочувствие, устраняются головные боли и головокружения, шум в ушах и другие симптомы, связанные с заболеванием.
Необходим полный пересмотр рациона питания, в том числе и для коррекции лишнего веса, нередко сопутствующего гипертензии и сбоям кровоснабжения, терапия дополняется режимными моментами, дозированными физическими нагрузками и физиотерапией, психопрофилактическими мероприятиями, седативной терапией и устранением возможных когнитивных расстройств (упражнения для тренировки памяти, мышления, чтение книг, разгадывание кроссвордов).
Острые нарушения мозгового кровообращения: симптомы и лечение
При появлении острой головной боли, онемения части тела, паралича лица, конечностей, недомогания, потери сознания и тошноты, рвоты, необходимо немедленно вызвать скорую помощь, доставить пациента в стационар и не предпринимать никаких попыток самолечения, тем более при помощи народной медицины или различных нетрадиционных методов. Может быть потеряно драгоценного времени, что грозит необратимыми последствиями.
В остром периоде все необходимые мероприятия проводятся стационарно, но в дальнейшем велика роль родственников и самого человека, пострадавшего от проблем.
При нарушении мозгового кровообращения лечение и препараты подбираются индивидуально. В соответствии с клиническими стандартами используются следующие
группы лекарственных средств:
- нейропротекторы, способствующие восстановлению работоспособности клеток;
- седативные, устраняющие стресс и переживания, страх смерти и инвалидности;
- поливитаминные, особенно содержащие комплексы витаминов группы В, способствующие восстановлению нервной проводимости тех участков, которые частично взяли на себя функции пострадавших областей;
- препараты венотонизирующего действия, нормализующие отток крови по венозным сосудам и уменьшающие отечность головного мозга;
- средства с вазодилатирующим (сосудорасширяющим) эффектом;
- антиоксиданты, помогающие в защите клеток от гипоксии и воздействия свободнорадикальных и агрессивных соединений.
Действие всех лекарственных средств направлено на улучшение состояния клеток путем защиты от гипоксии и повреждения, улучшения питания и работы.
Дозировки и конкретное сочетание подбирается врачом, исходя из возраста пациента, степени тяжести заболевания и общего состояния больного.
Важно учитывать наличие сопутствующей патологии и причины, ставшей пусковым моментом в болезни: восстановление будет длительным и поэтапным, после выписки из стационара необходим период реабилитации и затем — поддерживающая терапия на протяжении всей жизни.
Последующее лечение при заболевании
Итак, напряженный период позади, и после выписки из стационара встает вопрос о том, чем лечить нарушение мозгового кровообращения в дальнейшем, на этапе восстановления.
Необходимо постоянный, в том числе и медикаментозный контроль за уровнем артериального давления и свертываемостью, общим состоянием и функциями внутренних органов.
Начиная с ранней реабилитации, еще в стационаре, и затем дома или в условиях санатория, показан курс лечебной физкультуры, помогающий в восстановлении нарушенных двигательных функций, координации движений и мышечного тонуса после длительного постельного режима.
Курс может включать:
- лечебный массаж;
- ортопедическую коррекцию;
- психотерапию.
ХНМК: лечение
При наличии постоянных или преходящих симптомов хронического нарушения мозгового кровообращения, лечение будет длительным, пожизненным и направленным на замедление прогрессирующих изменений в черепной коробке, связанных с гипоксией и дефицитом питания клеток.
Важно проводить все мероприятия для защиты нейронов от свободных радикалов и гипоксических поражений, активизировать метаболические процессы на уровне коры и подкорковых, стволовых образований, нормализовать ток крови по сосудам.
Препараты врач подбирает индивидуально, прием их осуществляется строго под контролем жизненных показателей.
Помимо базовой терапии, пациентам, имеющим плохое, недостаточное кровообращение головного мозга, лечение можно дополнить (только по согласованию с врачом или в соответствии с его назначениями) применением средств народной медицины и фитотерапии. С основными медикаментами рекомендованы растительные лекарства — сборы трав для нормализации тонуса сосудов и кровотока, средства природного происхождения — продукты пчеловодства.
Показана диета с уменьшением калорийности пищи для борьбы с лишним весом и мероприятия по снижению общего холестерина и атерогенных жиров (липопротеинов низкой и очень низкой плотности). При неэффективности только пищевой коррекции показаны специальные препараты группы статинов, назначаемые на длительный срок.
Методы реабилитации и восстановительное лечение нарушения мозгового кровообращения
Лекарства могут остановить прогресс заболевания, но восстановить способности к движению или когнитивные функции лекарства не в силах. Поэтому важно проведение курса реабилитации, который поможет в устранении или уменьшении выраженности проблем с конечностями, движением и атрофией мышц.
Большую роль в реабилитации пациентов с ОНМК играют физиотерапевтические процедуры: магнитотерапия для улучшения кровотока в сосудах головного мозга и шеи, электромиостимуляция для восстановления утраченного тонуса мышц, гипербарическая оксигенация (барокамера) для увеличения доступа кислорода в клетки мозга.
При восстановлении для возвращения утраченных функций организма нужно терпение и упорство самого человека и его родных, которым придется проводить специальные курсы массажа и гимнастики на протяжении нескольких месяцев.
Существует классическая система упражнений, проводимых при помощи рук человека или тренажеров, помогающая в обучении новым моделям движения, формирующая новые условно-рефлекторные связи в мозге.
По сути человек заново учится двигаться, поддерживать равновесие и тонус мышечных групп. В разработке восстановительного лечения участвуют врачи-реабилитологи, кинезиотерапевты, массажисты и неврологи.
Специалисты подбирают индивидуальную программу, следят за ее переносимостью и прогрессом в восстановлении функций.
Дополнительные реабилитационные мероприятия
По мере устранения острых симптомов терапия дополняется дыхательной гимнастикой, проводимой прямо в постели по мере улучшения состояния пациента. Комплекс упражнений направлен на улучшение оксигенации тканей, в том числе и мышц, на снятие мышечного напряжения после гимнастики и массажа, улучшения общего эмоционального тонуса.
При наличии длительного постельного режима препараты дополняют полноценные мероприятия по уходу, необходимые для профилактики серьезных осложнений – застойной пневмонии, контрактур суставов и пролежней.
Важно постоянно менять положение больного, в том числе с переворотами на живот, а также необходимо подкладывание валиков и подушек под ноги и спину.
Использование в процессе ухода специальных гигиенических средств, косметических препаратов, медицинских приспособлений позволяет сохранять в хорошем состоянии кожные покровы лежачего больного.
Источник: https://Elamed.com/dr/stati/kak-lechit-narushenie-mozgovogo-krovoobrashheniya/
Популярные статьи на Доктор ЕЛАМЕД:
Как лечить артроз: современные способы и методы лечения суставов
Как вылечить ревматоидный артрит
Алмаг-01 – плацебо или лечебный аппарат?
Источник: https://zen.yandex.ru/media/dr_elamed/kak-lechit-narushenie-mozgovogo-krovoobrasceniia-5acb49019e29a2658dfd77e0
Газета «Новости медицины и фармации» 7 (409) 2012
Сосудистые заболевания головного мозга остаются одной из острейших и глобальных медико-социальных проблем, наносящих огромный экономический ущерб обществу.
В Украине львиная доля (95 %) цереброваскулярных заболеваний (ЦВЗ) принадлежит хроническим нарушениям мозгового кровообращения, рост частоты встречаемости которых в основном и предопределяет увеличение распространенности ЦВЗ в нашей стране.
Тенденция к постарению населения планеты и увеличение в популяции числа основных факторов риска развития сосудистых заболеваний головного мозга (артериальная гипертензия (АГ), болезни сердца, сахарный диабет (СД), гиперхолестеринемия, гиподинамия, курение и другие) обусловливают дальнейший рост ЦВЗ на ближайшие десятилетия [1–5].
Известно, что важнейшим независимым фактором риска развития всех форм ЦВЗ является сахарный диабет — одно из самых распространенных заболеваний среди людей среднего и пожилого возраста. СД поражает в среднем от 1,2 до 13,3 % населения планеты и является причиной около 4 млн смертей ежегодно во всем мире.
Наиболее часто в структуре СД (90–95 %) встречается сахарный диабет 2-го типа. По оценкам Всемирной организации здравоохранения, число лиц, страдающих сахарным диабетом, в мире составляет более 190 млн, а к 2025 году эта цифра возрастет до 330 млн. В Украине на сегодняшний день зарегистрировано более 1 млн пациентов, страдающих сахарным диабетом.
Однако данные эпидемиологических исследований показали, что истинное число больных в 2–2,5 раза выше [2–5].
На основании проведенных широкомасштабных исследований было установлено, что СД повышает риск развития мозгового инсульта в 2–6 раз, транзиторных ишемических атак — в 3 раза по сравнению с таковым риском в общей популяции.
Кроме того, СД отводится важная роль в формировании хронической прогрессирующей недостаточности мозгового кровообращения — диабетической энцефалопатии (ДЭ) и сосудистой деменции.
Риск развития сердечно-сосудистых катастроф значительно увеличивается при сочетании СД с другими факторами риска (АГ, дислипидемия, ожирение), что нередко наблюдается у данной когорты пациентов [3, 5–8].
Патогенетическую основу развития ЦВЗ у больных с диабетом обусловливает генерализованное поражение при СД мелких сосудов (микроангиопатия), сосудов среднего и крупного калибра (макроангиопатия).
В результате развивается так называемая диабетическая ангиопатия, наличие и выраженность которой определяют течение и прогноз заболевания.
Установлено, что изменения в мелких сосудах (артериолах, капиллярах, венулах) носят специфический для СД характер, а в крупных — расцениваются как ранний и распространенный атеросклероз [2–4, 9, 10].
Патогенез микроангиопатии (в том числе vasa nervorum) при диабете связан с образованием аутоантител к гликозилированным белкам сосудистых стенок, накоплением в сосудистой стенке липопротеидов низкой плотности, активизацией процессов перекисного окисления липидов и увеличением образования свободных радикалов, подавлением синтеза простациклина и дефицитом оксида азота, обладающих антиагрегантным и сосудорасширяющим действием.
Развитие дислипидемии на фоне повышения проницаемости сосудистой стенки за счет ее структурных нарушений, связанных с гликозилированием белковых молекул, усилением процессов пероксидации, дефицитом NO и др.
, приводит к формированию атеросклеротических бляшек, поражающих магистральные сосуды (макроангиопатия). При этом диабетическая макроангиопатия не имеет специфических отличий от атеросклеротических изменений сосудов у людей без СД.
Однако установлено, что атеросклероз при СД развивается на 10–15 лет раньше, чем у лиц без него, и затрагивает большинство артерий, что объясняется метаболическими нарушениями, предрасполагающими к сосудистым поражениям [4, 5, 9, 10].
Кроме того, более широкой распространенности атеросклеротического процесса при СД способствует и развитие микроангиопатий.
В свою очередь, прогрессирование микро- и макроангиопатий приводит к снижению эндоневрального кровотока и тканевой гипоксии. Развивающаяся при этом дисгемическая гипоксия переключает энергетический метаболизм нервной ткани на малоэффективный анаэробный гликолиз.
В результате в нейронах снижается концентрация фосфокреатина, возрастает содержание лактата (продукт анаэробного окисления глюкозы), развиваются энергетический дефицит и лактоацидоз, что приводит к структурно-функциональным нарушениям в нейронах, клиническим результатом чего является развитие диабетической энцефалопатии.
Диабетическая энцефалопатия — стойкая церебральная патология, возникающая под воздействием хронической гипергликемии, метаболических и сосудистых нарушений, клинически проявляется неврологическими синдромами и психопатологическими расстройствами.
Установлено, что важную роль в развитии хронических нарушений мозгового кровообращения при СД играют также эндотелиальная дисфункция, нарушение ауторегуляции мозгового кровотока, повышение вязкости и агрегационных свойств крови [5, 6, 10, 11].
Известно, что адекватное функционирование процессов ауторегуляции мозгового кровотока способно компенсировать гемодинамический дефицит, обусловленный различными причинами, за счет сочетанной работы анатомических и функциональных источников компенсации.
По мнению ряда авторов, низкие показатели цереброваскулярной реактивности ассоциируются с повышенным риском развития острых и хронических нарушений мозгового кровообращения [12–15]. Ауторегуляция церебрального кровообращения обеспечивается комплексом миогенных, метаболических и нейрогенных механизмов.
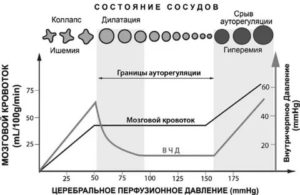
Миогенный механизм связан с реакцией мышечного слоя сосудов на уровень внутрисосудистого давле- ния — так называемый эффект Остроумова — Бейлиса. При этом церебральный кровоток поддерживается на постоянном уровне при условии колебания среднего артериального давления (АД) в диапазоне от 60–70 до 170– 180 мм рт.ст.
за счет способности сосудов реагировать: на повышение системного АД — спазмом, на снижение — дилатацией. При снижении АД менее 60 мм рт.ст. или подъеме выше 180 мм рт.ст. появляется зависимость «АД — мозговой кровоток», за которой следует «срыв» ауторегуляции церебрального кровообращения.
Метаболический механизм ауторегуляции опо- средован тесной связью кровоснабжения головного мозга с его метаболизмом и функцией. Метаболическими факторами, обусловливающими интенсивность кровоснабжения мозга, являются уровни РаСО2, РаО2 и продуктов метаболизма в артериальной крови и ткани мозга.
Снижение нейронального метаболизма приводит к снижению уровня мозгового кровотока.
Таким образом, ауторегуляция мозгового кровотока — легкоуязвимый процесс, который может нарушаться при резком повышении или снижении АД, гипоксии, гиперкапнии, прямом токсическом действии экзо- и эндотоксинов на мозговую ткань, в том числе хронической гипергликемии и каскада патологических процессов, которые она инициирует. В этом случае срыв ауторегуляции является составной частью патологического процесса при СД, на основе которого формируются хронические нарушения церебральной гемодинамики и диабетическая энцефалопатия. А оценка состояния цереброваскулярного резерва имеет важное прогностически-диагностическое значение для форм ЦВЗ диабетического генеза [12–15].
Целью настоящего исследования явилось определение роли нарушения вазомоторной реактивности сосудов мозга в формировании диабетической энцефалопатии и разработка путей ее коррекции.
Материалы и методы
Было обследовано 67 больных с СД 2-го типа в стадии субкомпенсации и диабетической энцефалопатией в возрасте от 48 до 61 года и длительностью диабета от 4 до 11 лет, находившихся на лечении в неврологическом отделении Научно-практического медицинского центра ХНМУ.
У 24 (35,8 %) больных была установлена легкая степень СД, у 32 (47,8 %) — средняя степень тяжести, у 11 (16,4 %) пациентов — тяжелая форма СД.
45,6 % обследованных пациентов в качестве гипогликемической терапии получали инсулинотерапию, 54,4 % больных — таблетированные сахароснижающие препараты.
https://www.youtube.com/watch?v=wHjWj5Rz7oQ
Состояние церебральной гемодинамики и сосудистой реактивности артерий мозга изучалось по стандартным методикам с использованием датчиков частотой 2, 4, 8 МГц на аппарате «Спектромед-300» (Россия). Алгоритм исследования состояния церебральной гемодинамики и вазомоторной реактивности включал:
Ø исследование магистральных артерий головы и интракраниальных артерий методами экстра- и интракраниальной допплерографии с определением скоростных характеристик кровотока, индексов пульсации и циркуляторного сопротивления;
Ø исследование вазомоторной реактивности по результатам компрессионного теста.
Известно, что кратковременная пальцевая компрессия общей сонной артерии (ОСА) на шее приводит к снижению перфузионного давления и развитию преходящего гиперемического ответа после прекращения компрессии, что позволяет рассчитать ряд показателей, характеризующих резервы ауторегуляции.
Пациентам (с отсутствием стенозирующего поражения сонных артерий) проводили 5–6-секундную компрессию ОСА с прекращением компрессии в фазу диастолы.
Регистрировали среднюю линейную скорость кровотока (ЛСК) в средней мозговой артерии (СМА) до компрессии ипсилатеральной ОСА — V1, во время компрессии — V2, после прекращения компрессии — V3, а также время восстановления исходной ЛСК — T (рис. 1). С помощью полученных данных рассчитывали коэффициент овершута (КО) по формуле: КО = V3/V1 [15].
Полученные данные были статистически обработаны с использованием пакета прикладных статистических программ Statistica 6.0. Рассчитывались средние значения показателей и ошибки средних. В качестве критерия значимости различия выборок использовались параметрические и непараметрические критерии Стьюдента и Уилкоксона. Различия принимались достоверными при р < 0,05.
Результаты исследования и их обсуждение
В ходе клинико-неврологического обследования больных с СД 2-го типа диабетическая энцефалопатия I степени была диагностирована у 29 пациентов (43,3 %), диабетическая энцефалопатия II степени — у 38 больных (56,7 %).
Ведущими неврологическими синдромами у обследованных были: цефалгический синдром (96,5 % случаев); статико-координаторные нарушения (86,1 %); психоэмоциональные расстройства от эмоциональной лабильности до депрессивных синдромов (89,5 %); когнитивная дисфункция (89,5 %); внутричерепная гипертензия (84,2 %), пирамидная недостаточность по центральному типу (49,1 %), полиневропатический синдром (96,5 %), нарушение сна (66,7 %) и др. Цефалгический синдром в большинстве случаев (в 87,7 %) имел сосудистый генез (головные боли носили давящий характер, височную или лобно-височную локализацию, усиливались при смене метеоусловий и психоэмоциональном перенапряжении) или смешанный генез в комбинации с внутричерепной гипертензией (цефалгии распирающего характера с чувством давления изнутри на глазные яблоки и симптомами гиперестезии). Частым неврологическим синдромом при диабетической энцефалопатии были когнитивные нарушения легкой (27–26 баллов по шкале MMSE) и умеренной степени выраженности (25–24 балла по шкале MMSE). Следует отметить, что частота и выраженность объективной симптоматики у обследованных нарастали по мере прогрессирования тяжести диабетической энцефалопатии. Соматическое обследование больных с СД выявило сопутствующую артериальную гипертензию, преимущественно 2-й степени (86 % случаев), длительность которой составляла в среднем 12,3 ± 3,5 года; гиперхолестеринемию (82,5 %); избыточный вес (40,4 %).
Нарушение церебральной гемодинамики у больных с СД 2-го типа по данным допплерографического исследования характеризовалось снижением скорости кровотока в ВСА на 24,5 и 33,9 %, в СМА — на 25,4 и 34,5 %, в ПА — на 24,3 и 44,7 %, в ОА — на 21,7 и 32,6 % (при ДЭ I и II степени соответственно) по отношению к показателям в контрольной группе. Также были выявлены признаки повышения сосудис- того тонуса во всех исследованных сосудах по данным повышения индекса пульсации (Pi) и циркуляторного сопротивления (Ri) в среднем в 1,5 и 1,3 раза при ДЭ I степени и в 1,8 и 1,75 раза при ДЭ II степени. Гемодинамических значимых стенозов магистральных артерий головы у обследованных больных не было выявлено ни в одном случае (их наличие было критерием исключения из исследования в силу опасности проведения компрессионных проб).
Снижение возможностей коллатерального кровотока (анатомического звена церебрального сосудистого резерва) у обследованных пациентов с диабетической энцефалопатией I и II степени подтверждалось депрессией относительно контрольных показателей остаточной скорости кровотока в СМА (V2) в момент компрессии ипсилатеральной ОСА на 19,3 и 28,1 % соответственно. Это отражало нарушение проходимости перфорирующих и соединительных артерий, возможно, в результате их вторичной облитерации как проявление атеросклеротической и диабетической ангиопатии. Снижение коэффициента овершута у больных с диабетической энцефалопатией I и II степени относительно контроля на 11,6 и 16,9 % соответственно свидетельствовало о напряжении функционального звена цереброваскулярной реактивности, в частности, ее миогенного компонента вследствие нарушения при СД структуры сосудистой стенки и ее тонуса. Выявленное увеличение в 1,7 и 2,3 раза времени восстановления скорости кровотока до исходной отражало нарушение мета- болического контура сосудистой реактивности как проявление общих дисметаболических процессов, развивающихся в организме при СД, — нарушения полиолового пути окисления глюкозы, избыточного накопления сорбитола и про- оксидантов, развития гиперлипидемии, дефицита депрессорных факторов, необратимого гликозилирования белков, в том числе белков стенок сосудов [4, 6, 8, 11].
Следует отметить, что выявленное ухудшение гемодинамических показателей и показателей цереброваскулярной реактивности у больных с СД 2-го типа находилось в прямо пропорциональной зависимости от степени тяжести диабетической энцефалопатии, что свидетельствовало о патогенетической роли нарушения ауторегуляции мозгового кровотока в развитии мозговых дисциркуляций и формировании энцефалопатического синдрома при СД 2-го типа.
Таким образом, нарушение церебральной гемодинамики и снижение реактивности сосудов головного мозга у пациентов с СД 2-го типа являются патогенетической основой формирования диабетической энцефалопатии.
Учитывая тесную связь гемодинамических и обменных нарушений при СД, а также их комплексную роль в патогенезе развития цереброваскулярных и неврологических осложнений сахарного диабета, в схемы терапии диабетической энцефалопатии необходимо включать препараты комплексного действия, способные улучшить состояние цереброваскулярной реактивности, уменьшить явления вазоспазма в церебральных сосудах и нормализовать метаболические процессы в организме, что позволит улучшить состояние пациентов с СД и качество их жизни.
Источник: http://www.mif-ua.com/archive/article/28874






